Association Saint Louis pour la recherche sur les Leucémies |
|
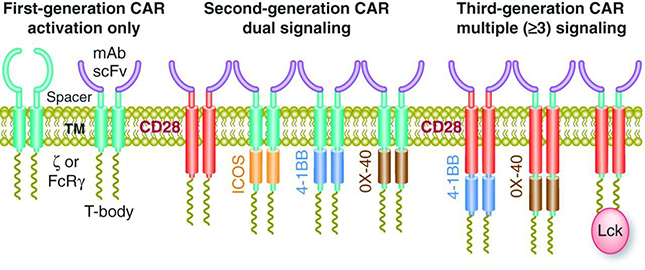
CAR T-cells : Une avancée majeure dans l’immunothérapie des leucémies ?Combattre la leucémie en utilisant les armes immunologiques (anticorps, lymphocytes) est une idée ancienne, qui a déjà connu un accomplissement dans la greffe de moelle osseuse. L’efficacité de la greffe repose en effet sur l’action des lymphocytes du donneur, qui sont présents dans le greffon et qui vont s’attaquer aux cellules leucémiques. Le recours à un donneur « allogénique » (identifié au sein de la famille ou dans un fichier de donneurs volontaires) nécessite néanmoins, même si le donneur est choisi pour sa relative compatibilité, de détruire le système immunologique du patient receveur pour éviter le rejet. Il nécessite aussi de contrôler la réactivité des lymphocytes transplantés pour en limiter les effets néfastes sur d’autres organes (maladie du greffon contre l’hôte). L’utilisation de lymphocytes T autologues, c’est-à-dire du patient lui-même, capables de reconnaitre spécifiquement les cellules leucémiques, peut permettre de résoudre une bonne partie de ces problèmes. Cette idée brillante de transformer un lymphocyte T en médicament « vivant » a donné le jour aux CAR T-cells, dont l’activité clinique vient d’être confirmée dans la leucémie aiguë lymphoblastique (LAL) par plusieurs équipes américaines. Les CAR T-cells (pour cellules T porteuses d’un récepteur chimérique) sont des lymphocytes T du patient, prélevés au patient, puis modifiés génétiquement in vitro de manière à leur faire exprimer un récepteur artificiel, dit chimérique. Ce récepteur est conçu de telle manière que sa partie extra-cellulaire reconnaisse un antigène tumoral, le plus spécifiquement possible afin d’éviter les effets néfastes sur d’autres organes du patient. En ce sens, l’antigène CD19 de la LAL représente un modèle très performant. La partie intra-cellulaire va, elle, se charger de l’activation des lymphocytes après fixation sur les cellules leucémiques : elle se compose de plusieurs domaines d’activation et de co-activation. Ces constructions ont évolué avec le temps pour donner naissance à plusieurs « générations » de CAR T-cells (Figure 1). Les premiers essais et premiers résultats cliniques dans la LAL sont apparus en 2012-2013, et ils sont extraordinaires. Trois équipes américaines (Penn University, National Cancer Institute, Memorial Sloan Kettering) ont rapporté les résultats de trois études indépendantes, menées chez des patients présentant des cellules leucémiques persistantes après traitement standard et parfois après allogreffe. Plusieurs dizaines de patients ont été traités. Les résultats sont concordants :
Le présent et le futur proche vont connaitre de nombreux essais cliniques destinés à confirmer ces premiers résultats, à améliorer encore les produits cellulaires utilisés, et à cibler d’autres leucémies et tumeurs solides.
Trois générations de CAR T-cells
|
|